概要
 がんの放射線治療では、放射線と照射する人体との相互作用による物理反応から、化学反応、生物反応が連鎖し、腫瘍細胞を殺傷します。医学物理学とは基礎物理学を基盤とする、放射線物理学、原子核物理学、原子・分子物理学、放射線計測学、電磁気学、物理数学、情報工学、医学、生物学などの幅広い学問の結集体であり、その知識及び成果を医学へ展開する学術分野が医学物理学分野です。
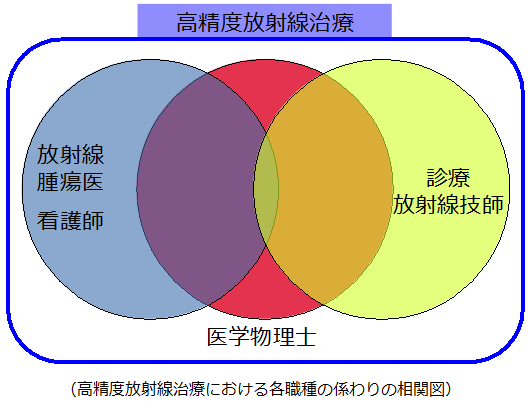
がんの放射線治療では、放射線と照射する人体との相互作用による物理反応から、化学反応、生物反応が連鎖し、腫瘍細胞を殺傷します。医学物理学とは基礎物理学を基盤とする、放射線物理学、原子核物理学、原子・分子物理学、放射線計測学、電磁気学、物理数学、情報工学、医学、生物学などの幅広い学問の結集体であり、その知識及び成果を医学へ展開する学術分野が医学物理学分野です。放射線治療が高度化する一方、その治療装置や技術の品質保証及び管理の項目は、より一層の複雑化を招いています。その結果、治療装置や技術の品質保証及び管理の業務は非常に幅広い領域で多岐に渡っており、現場の医療従事者の負担増になっています。そのため、それらの業務の中心的役割を担う人材が必要となります。また、放射線治療の高精度化には、医学物理学の研究開発が重要です。それ故に、大学や研究所においては革新的な医学物理学研究及び開発、研究者の育成を主体的に実施する人材が必要です。それらの業務を専従で実施するのが医学物理士であり、国内初の医学物理学の専門分野であるの当大学の医学物理学分野では、臨床現場や大学・研究所で活躍出来る医学物理士の研究教育と人材育成を目指します。尚、2018年より本学大学院医学物理学分野における医学物理士養成コースは一般財団法人医学物理士認定機構が定める講義基準・臨床基準の条件を満たす教育コースとして認定を受けております。( http://www.jbmp.org/course_educational/decision/ )
研究可能テーマ
 放射線治療の中核を担う装置の一つである治療計画装置は、海外メーカーが完全に主流となっている問題があります。そこで、陽子線、炭素線、Vero、Cygnusなどの国産放射線発生装置と連携し発生装置の最高のポテンシャルを引き出した放射線治療を実現するために国産放射線治療計画装置:jPRAPs(Japan Plug-in based Radiotherapy Planning System)の研究開発を行っています。プラグイン形式を採用するプラットホームを開発することで様々な機能を利用できる拡張性の高い装置の構築を目指しています。
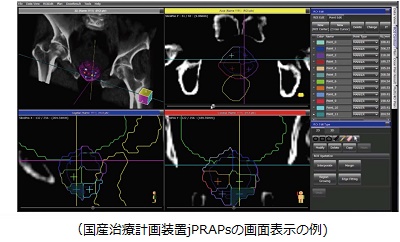
放射線治療の中核を担う装置の一つである治療計画装置は、海外メーカーが完全に主流となっている問題があります。そこで、陽子線、炭素線、Vero、Cygnusなどの国産放射線発生装置と連携し発生装置の最高のポテンシャルを引き出した放射線治療を実現するために国産放射線治療計画装置:jPRAPs(Japan Plug-in based Radiotherapy Planning System)の研究開発を行っています。プラグイン形式を採用するプラットホームを開発することで様々な機能を利用できる拡張性の高い装置の構築を目指しています。
高速高精度の線量計算アルゴリズムを研究開発することで放射線治療の更なる高精度化、また、病理画像と放射線治療を融合させた新たな病理画像支援放射線治療法の確立を目指しています。
「物理量検証用ツールの研究開発」
現在、放射線治療の線量などの物理量を検証する海外製ツールが市販されているが、簡便性と検証精度を兼ね備え、医療現場のニーズに適したツールとなっていない場合があります。そのため、医療現場から放射線治療の照射方法に適した高い精度の線量検証が実施可能な、ファントム、計測機器、解析ソフト等の物理量検証ツールの考案と研究開発、そしてその製品化により数多くの臨床施設へ提供することが重要です。 本研究では、これまでに培ってきた放射線計測技術を主軸とする多種多様の技術を駆使した物理量検証ツールを研究開発することで、多施設の放射線治療の高品質化の支援を目指します。

「放射線性皮膚反応を予測再現する技術開発」
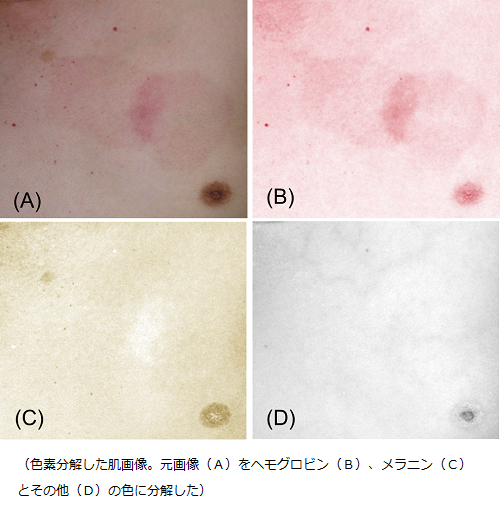
外部放射線治療は侵襲性の少ない治療です。しかし全くゼロというわけではなく、治療したい腫瘍が体内の奥深くにある限りは放射線の通り道となる正常組織の被ばくは避けることができません。例えば皮膚です。治療中の患者さんにとって放射線による皮膚反応は気になるものです。そこで我々は図のように肌画像をデジタル画像上で色素分解することで、皮膚の紅斑の度合いだけが変化すると単純化した時の皮膚反応を予言できることを示しました。今後は色素沈着や肌水分量変化の情報も加味して治療前に治療後の皮膚反応を予言できる開発を進めていきます。
「荷電粒子線治療に特化した生体内用小型線量計の開発」
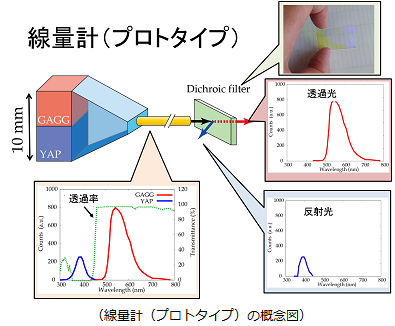
荷電粒子線治療(陽子線、もしくは炭素線治療)はブラッグピークを有する性質のおかげで線量を集中させた安全な治療が可能な反面、照射位置を誤ると正常組織に過剰線量が照射される危険を伴う治療であるともいえます。本研究ではそのような危険性を照射中に感知できるよう、光ファイバーとシンチレータを組み合わせた生体内に挿入な可能な超小型線量計の開発を目指しています。X線治療用とは異なりブラッグピークにおける高線量領域のクエンチング現象による測定精度劣化の問題があるため、二種類のシンチレータの色情報(発光波長)と線量応答の違いを利用してこの問題を克服する世界で初めての新しい小型線量計の開発を進めています。
「4次元ビーム照射方向計測システム(こんぺいとうショットシステム)の研究開発」
 IMRTやVMAT、SBRTといった高精度放射線治療の実施には、高いビーム照射位置精度が必要となります。しかし、従来の品質管理手法ではガントリ回転軸方向(患者頭足方向)の定量評価が難しいという問題があります。また、追尾照射が可能なVero4DRTやCyberKnifeは、ビーム照射軸が1点で交わるisocentrer(照射中心位置)を基準とした照射ではないという特徴があります。それゆえ、照射中心位置からのシフト量を評価する従来法では、満足のいく測定・評価ができません。
IMRTやVMAT、SBRTといった高精度放射線治療の実施には、高いビーム照射位置精度が必要となります。しかし、従来の品質管理手法ではガントリ回転軸方向(患者頭足方向)の定量評価が難しいという問題があります。また、追尾照射が可能なVero4DRTやCyberKnifeは、ビーム照射軸が1点で交わるisocentrer(照射中心位置)を基準とした照射ではないという特徴があります。それゆえ、照射中心位置からのシフト量を評価する従来法では、満足のいく測定・評価ができません。私たちが開発を進める新規品質管理手法では、3次元空間内におけるビーム照射軸そのものを測定することが可能です。したがって、照射中心位置からのシフト量の定量評価はもちろんのこと、最新の治療機の品質管理にも対応できると考えています。
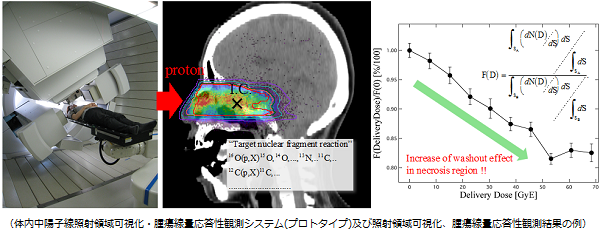
「体内中陽子線照射領域可視化・腫瘍線量応答性観測システムの研究開発」
放射線は目に見えないために実際の陽子線治療では腫瘍へ的確に照射されたかを確認出来ていない問題点がありました。そこで、本研究では入射陽子と患者体内中の人体構成原子核との標的原子核破砕反応による生成ポジトロン放出核を情報因子とすることで体内中照射領域可視化システムの研究開発を行っています。更に標的原子核破砕反応により腫瘍内で生成されるポジトロン放出核の位置及び強度の時間的変化を観測することで、照射線量に対するそれらの時間的変化に法則があることを観測しました。本システムの研究開発を進めることで、腫瘍へ的確に陽子線を照射することが可能となり、また、腫瘍の線量応答性を把握出来る可能性があり、患者個別に対する最適な処方線量による新たなテーラーメイド陽子線治療への実現が期待出来ます。
「陽子線CT画像取得システムの研究開発」
ブラッグピークを活用する陽子線治療では患者体表と腫瘍までの距離に対応する飛程の計算精度が重要となります。現在、X線CT画像を用いた陽子線飛程計算では3%の計算誤差が存在すると言われています。本研究では治療と同じ線種である陽子線を用いたCT画像によって飛程精度問題を解決するために、陽子線CT画像を取得可能な新たな計測システムを開発しました。本システムを用いることで、世界で初めて複雑な構造をした物体の画像化に成功しました。本システムを活用し、様々な条件での陽子線CT画像の取得と得られたデータの詳細解析を進めることで、陽子線の体内中飛程の計算精度の向上を目指しています。

「陽子線スキャニング照射の治療計画最適化」
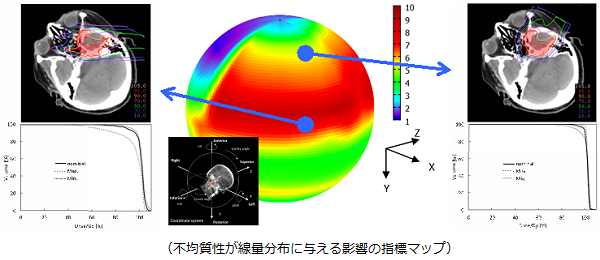
陽子線治療のスキャニング照射は、加速器から送られてきた細い陽子ビームを、電磁石を用いてビームの方向を変え、がんの病巣を塗りつぶすように照射する最先端の技術です。従来の方式に比べて腫瘍の線量集中性を高めながら健康な組織への線量を減少させることができ、「からだにやさしいがん治療」が可能になります。一方で、陽子ビームは体内の不均質性の影響を受けて分布が乱れることがあり、それを考慮して治療計画のパラメータ(照射する方向、ビームのサイズ、粒子数など)を決めることが大切です。それぞれの患者さんにとって、スキャニング照射技術を最大限に活用した治療ができるよう、治療計画の最適化の研究開発を進めています。
「小型陽子線治療装置の研究開発」
陽子線治療を国内外へ広く普及させるために必要不可欠となる装置の小型化研究開発(現在の装置は約テニスコート一面分の大きさ)が重要となります。本分野が医学物理学研究の中核拠点となり、早稲田大学の医理工連携を主軸にした研究開発を展開することで、小型で高性能な陽子治療装置の研究開発を進めています。
スタッフ紹介
助教:寅松 千枝・(茨城大、博士(理学);医学物理士)
助教:松原 礼明・(大阪大、博士(理学);医学物理士)
助教:恒田 雅人・(広島大、博士(医学);医学物理士)


(左から、松原、西尾、寅松、恒田) (医学物理学分野スタッフ及び大学院生)
助教:松原 礼明・(大阪大、博士(理学);医学物理士)
助教:恒田 雅人・(広島大、博士(医学);医学物理士)


(左から、松原、西尾、寅松、恒田) (医学物理学分野スタッフ及び大学院生)
最先端の医学物理学研究
本大学院では、医学物理学研究及び教育体制が充実しており、産学官連携による最先端の医学物理学研究を展開している特徴があります。また、理学、工学及び放射線技術学系の他大学との連携、医療系メーカーとの共同研究、科研費や国プロによる大規模な医学物理学研究を推進しています。
本大学院での医学物理学研究教育環境を活かし、医学物理学分野における世界のフラッグシップを取る研究成果と研究・教育から臨床現場で活躍できる医学物理士の人材輩出を目指します。
本大学院での医学物理学研究教育環境を活かし、医学物理学分野における世界のフラッグシップを取る研究成果と研究・教育から臨床現場で活躍できる医学物理士の人材輩出を目指します。


